Hipofosfatemia no uso da nutrição parenteral: qual a incidência e como deve ser o monitoramento da condição?
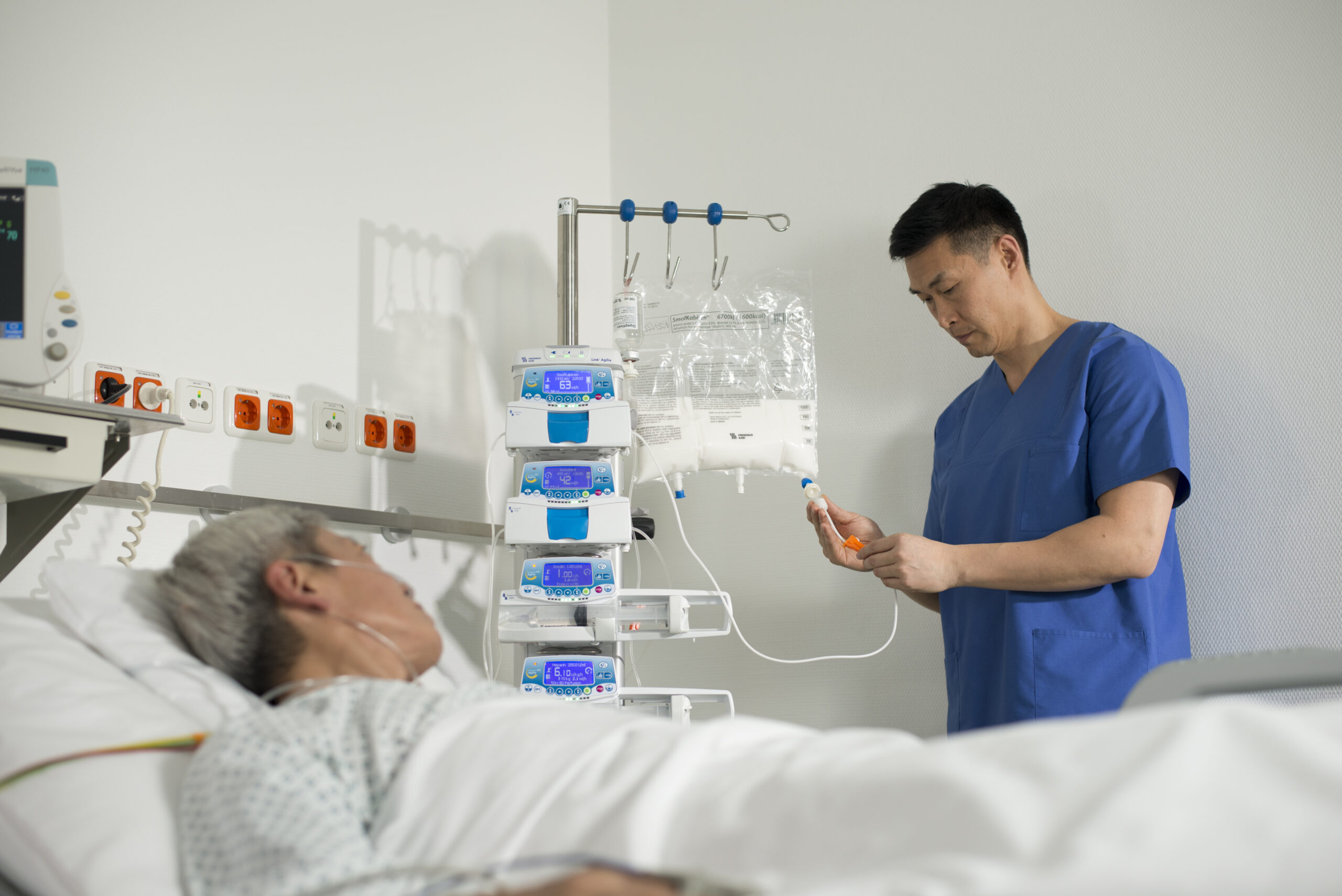
A hipofosfatemia é uma condição frequentemente associada à introdução da terapia nutricional, sobretudo na via parenteral. De todo modo, muitas incertezas ainda existem sobre a forma como deve se dar o manejo e o monitoramento dos indivíduos em risco e já afetados pelo desequilíbrio do fósforo.
Vale reforçar também que a hipofosfatemia (e, menos frequente, outros desequilíbrios eletrolíticos) costuma ser um marcador importante da chamada síndrome de realimentação1. Esse problema pode colocar em risco a vida dos pacientes e se manifesta com incidências variadas em diferentes circunstâncias. Isso reforça ainda mais a necessidade de uma abordagem multidisciplinar para dar conta desse problema1.
O que se sabe sobre a incidência de hipofosfatemia em pacientes recebendo nutrição parenteral?
Em geral, estima-se que a hipofosfatemia atinja entre 0,2% e 2,2% entre todos os pacientes admitidos em uma unidade hospitalar2. Contudo, já se sabe que a demanda de cuidados intensivos, a presença de quadros desconforto respiratório, infecção grave e a necessidade de nutrição enteral ou parenteral são condições associadas a uma elevação de 30% a 40% nas ocorrências desse problema3,4.
Com relação à introdução da nutrição parenteral, um estudo de 2016 mostrou que em uma amostra de 57 pacientes que receberam essa forma de suporte nutricional, a incidência de hipofosfatemia era de 39,6%. Nesse estudo foi considerado um patamar abaixo de 0,80 mmol/L para caracterizar a deficiência sérica. A monitorização foi feita em diferentes momentos antes e depois do início da administração da dieta via parenteral1.
O estudo acompanhou pacientes com idade média de 59,1 anos, em sua maioria homens (representando pouco mais de 60% da amostra)1. Em geral, a nutrição parenteral foi solicitada quando pacientes eram admitidos em unidades de terapia intensiva ou nas enfermarias cirúrgicas.
Assim, 41% da amostra apresentou risco de desenvolver a síndrome de realimentação, demandando, inclusive, uma taxa reduzida de infusão da nutrição parenteral1.
A hipofosfatemia, portanto, apresenta relação com a nutrição parenteral uma vez que ela costuma ser ofertada para o paciente já desnutrido, com mais chances de apresentar comprometimento nutricional e a síndrome de realimentação. Além disso, há o risco de a solução apresentar uma concentração baixa de fósforo,5,6.
De todo modo, cuidado semelhante deve ser tomado quando da introdução da nutrição enteral, pois essa terapia nutricional também apresenta forte relação com o risco de síndrome de realimentação7.
Que desfechos e complicações estão associados à hipofosfatemia?
Entre alguns dos comprometimentos mais comuns nesses quadros estão8:
- Prejuízo à função neuromuscular (com confusão mental, parestesias, entre outros sintomas);
- Insuficiência respiratória;
- Episódios de rabdomiólise (destruição de fibras musculares).
No mais, a queda de fosfato no organismo pode originar trombocitopenia, coagulopatia, disfunção leucocitária e eritrocítica8.
A síndrome de realimentação pode desencadear ainda o desequilíbrio de outros minerais. Isso tende a gerar casos de hipomagnesemia e hipocalemia, condições associadas a desfechos como arritmias cardíacas graves e alterações neuromusculares8.
Logo, todas essas mudanças, em conjunto com a desnutrição acentuada e prolongada, levam à atrofia cardíaca e tornam o coração mais vulnerável à hipofosfatemia e hipocalemia, elevando a chance de morte súbita7.
Para ilustrar isso, vamos recorrer mais uma vez aos números do estudo já citado no tópico anterior. Dentro da amostra analisada, 45,6% dos pacientes sob cuidados hospitalares recebendo intervenção nutricional foram à óbito1.
E os autores mostram que nesse pior desfecho os indivíduos apresentavam uma concentração de fósforo maior no início do acompanhamento1. Isso indica que a queda do fósforo sérico foi mais elevada nesse grupo, principalmente considerando o segundo e o terceiro dia após a introdução da nutrição parenteral1.
Além da hipofosfatemia, houve manifestações de hipomagnesemia (deficiência de magnésio), de hipocalemia (deficiência de potássio) e de hiponatremia (deficiência de sódio) em 28,1%, 7% e 8,8% dos pacientes, respectivamente1.
Qual a importância do monitoramento dessa condição e como fazer isso da forma adequada?
Profissionais de saúde que atuam no manejo de pacientes com comprometimento nutricional grave devem ter a ciência dos protocolos de cada instituição. A partir disso, o acompanhamento adequado desde o primeiro dia da admissão pode fazer toda a diferença na identificação dos pacientes sob risco de desenvolver a síndrome de realimentação1.
Assim sendo, é preciso considerar que a maioria dos quadros de síndrome de realimentação tende a ocorrer entre o terceiro e o quinto dia após o início da nutrição parenteral9. Logo, considerando o papel da hipofosfatemia na evolução da síndrome e como marcador de estágios precoces dessa complicação, a concentração de fósforo sérico tende a ser um indicador importante10.
No entanto, a hipofosfatemia associada à terapia nutricional possui diferentes pontos de corte da concentração sérica de fosfato1. Esses números geralmente variam de acordo com as evidências consultadas e não há definição universalmente aceita1.
Ao mesmo tempo, não é incomum que pacientes apresentem deficiências de fosfato antes mesmo do início da nutrição via enteral ou parenteral. Inclusive, no estudo analisado, 15,8% dos pacientes estavam nessa condição1.
Com isso, várias evidências sugerem que pacientes sob risco da síndrome de realimentação devem passar por monitorização diária de eletrólitos, sinais vitais e peso, sobretudo nas primeiras 72 horas após o início da terapia nutricional11.
Assim, o manejo de possíveis casos de hipofosfatemia envolve a correção do desequilíbrio, principalmente na presença de quadros graves ou que apresentam sintomas e sinais como arritmias, insuficiência cardíaca, fraqueza muscular e convulsões7,12-14.
Para mais informações sobre a administração da nutrição parenteral de forma mais segura e efetiva, continue navegando pelo Unidos Pela Nutrição Clínica.
Referências:
- Fung EC, Wickramasinghe SR, Panteli JV, Crook MA. Hypophosphataemia and parenteral nutrition; biochemical monitoring, incidence and outcomes. Br J Biomed Sci. 2017;74(1):48-51. Disponível em: <https://www.tandfonline.com/doi/full/10.1080/09674845.2016.1209896> Acesso em 20 de março de 2024.
- Gaasbeek A, Meinders AE. Hypophosphatemia: an update on its etiology and treatment. Am J Med. 2005 Oct;118(10):1094-1101. Disponível em: <https://www.amjmed.com/article/S0002-9343(05)00100-2/abstract> Acesso em 20 de março de 2024.
- Weinsier R. Death resulting from overzealous total parenteral nutrition: the refeeding syndrome revisited. Am J Clin Nutr. 1980;34(2):393–9.
- Llop Talaveron JM, Comas Sugranes D, Badia Tahull MB, Saez Fernandez A, Jodar Masanes R, Gomez Saez JM. Hypophosphatemia in parenteral nutrition: prevention and associated risk factors. Nutr Hosp. 2004;19(6):362–6.
- Fernandes VPI, da Costa Pinto EAL, Boin IDFSF, Nogueira RJN. Phosphorus levels during infusion of parenteral nutrition with calorie-based phosphorus concentration: a case series. e-SPEN Eur e-J Clin Nutr Metab. 2009;4(5):e252-e256. Disponível em: <https://clinicalnutritionespen.com/article/S1751-4991(09)00074-2/fulltext> Acesso em 11 de abril de 2024.
- Marinella MA. The refeeding syndrome and hypophosphatemia. Nutr Rev. 2003;61(9):320-3. Disponível em: <https://academic.oup.com/nutritionreviews/article/61/9/320/1907832?login=false> Acesso em 11 de abril de 2024.
- Zeki S, Culkin A, Gabe SM, Nightingale JM. Refeeding hypophosphataemia is more common in enteral than parenteral feeding in adult in patients. Clin Nutr. 2011;30(3):365-8. Disponível em: <https://www.clinicalnutritionjournal.com/article/S0261-5614(10)00213-X/abstract> Acesso em 20 de março de 2024.
- Friedli N, Stanga Z, Culkin A, Crook M, Laviano A, Sobotka L, et al. Management and prevention of refeeding syndrome in medical inpatients: an evidence-based and consensus-supported algorithm. 2018;47:13-20. Disponível em: <https://www.sciencedirect.com/science/article/abs/pii/S0899900717302071?via%3Dihub> Acesso em 20 de março de 2024.
- Crook MA, Hally V, Panteli JV. The importance of the refeeding syndrome. 2001;17:632–637. Disponível em: <https://www.sciencedirect.com/science/article/abs/pii/S0899900701005421?via%3Dihub>Acesso em 20 de março de 2024.
- A mixed bag. An enquiry into the care of hospital patients receiving parenteral nutrition. A report by the national confidential enquiry into patient outcome and death. London; 2010. Disponível em: <http://www.ncepod.org.uk/2010report1/downloads/PN_summary.pdf > Acesso em 20 de março de 2024.
- Aubry E, Friedli N, Schuetz P, Stanga Z. Refeeding syndrome in the frail elderly population: prevention, diagnosis and management. Clin Exp Gastroenterol. 2018;11:255-64. Disponível em: <https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6045900/> Acesso em 11 de abril de 2024.
- Rio A, Whelan K, Goff L. Occurrence of refeeding syndrome in adults started on artificial nutrition support: prospective cohort study. BMJ Open. 2013. Disponível em: <https://bmjopen.bmj.com/content/3/1/e002173.long> Acesso em 11 de abril de 2024.
- Schetz M, Casaer MP, van den Berge G. Does artificial nutrition improve outcomes of critical illness? Crit Care. 2013;17:302. doi:10.1186/cc11828. Disponível em: <https://ccforum.biomedcentral.com/articles/10.1186/cc11828> Acesso em 11 de abril de 2024.
- Shenkin A. Biochemical monitoring of nutrition support. Ann Clin Biochem. 2006;43:269–272. Disponível em: <https://journals.sagepub.com/doi/10.1258/000456306777695609?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed> Acesso em 11 de abril de 2024.