Generalidades del metabolismo del paciente crítico
Comprende las fases metabólicas en pacientes críticamente enfermos y cómo impactan las decisiones nutricionales en la unidad de cuidados intensivos.
El metabolismo del paciente crítico representa un desafío importante al momento de proporcionar una nutrición adecuada en la unidad de cuidados intensivos. Tradicionalmente, se consideraba que una nutrición temprana agresiva en las fases iniciales podría mejorar los resultados clínicos. Sin embargo, los resultados de estudios recientes no encontraron un beneficio superior con el inicio temprano de la nutrición. Parte de esta falta de beneficio puede deberse al impacto de la enfermedad grave temprana en el metabolismo.
El paciente en un estado de enfermedad aguda pasa por dos fases metabólicas: aguda inicial, que se caracteriza por un período de inestabilidad hemodinámica y cambios hormonales, entre ellos la resistencia a la insulina, que priorizan la entrega de sustratos de energía a los tejidos y aguda tardía, que involucra la destrucción de los tejidos con el fin de proveer sustratos para la respuesta de conservación del cuerpo, así como para disminuir los riesgos de infección o de sangrado.
Posterior a esto, se ha descrito una tercera fase anabólica de recuperación, en la que se realiza la reconstrucción de los tejidos y el empleo al máximo de los nutrimentos proporcionados.
La base de la respuesta metabólica al estrés es el reflejo de “lucha o huida”, una respuesta no específica destinada al mantenimiento de la homeostasis corporal. La respuesta involucra componentes neuroendocrinos e inmunoinflamatorios. Todo estímulo nocivo inicia una respuesta al nivel del hipotálamo, este activa el sistema nervioso simpático (SNS), mediante el eje hipotalámico-hipofisario-adrenal (HHA) para la liberación de noradrenalina al órgano blanco o al torrente sanguíneo.
Esto produce, como resultado final, un incremento de la gluconeogénesis (generación de glucosa a partir de otros sustratos), la glucólisis (degradación de glucosa), la movilización de los ácidos grasos y la proteólisis muscular con la liberación de aminoácidos.
Al pasar al estado subagudo de la enfermedad, los niveles de las hormonas hipofisarias disminuyen gradualmente, mientras persiste la resistencia a los efectos de la insulina, la hormona de crecimiento, la TSH y al cortisol. El componente inflamatorio de la respuesta al estrés es regulado, así mismo, a nivel del sistema nervioso central (SNC), mediante la liberación de citoquinas y mediadores proinflamatorios, que pueden impactar en los aspectos metabólicos del cuerpo. El factor de necrosis tumoral (TNF), la interleuquina (IL) 1 y la IL-6 provocan cambios en el medio interno durante el proceso séptico que inducen la pérdida de peso, un aumento de la proteólisis y la lipólisis, como parte de la respuesta a la infección.
Igualmente, producen anorexia a nivel del hipotálamo, como parte de una respuesta más grande denominada anorexia relacionada con la enfermedad. La respuesta final común al estrés, a nivel del metabolismo, involucra el aumento de la resistencia a los estímulos anabólicos, con el fin de redirigir los sustratos de energía hacia los órganos vitales y disminuir el consumo de glucosa de los órganos dependientes de insulina, como lo serían la grasa y el músculo.
Esta respuesta de resistencia a la insulina incluye, a su vez, una incapacidad de suprimir la producción hepática de glucosa y una disminución de la captación de glucosa de los tejidos periféricos mediante la disminución de las señales posteriores al receptor de insulina y de la expresión del glucotransportador 4 (GLUT-4):
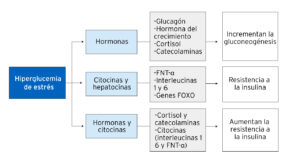
Alteraciones nutricionales en el paciente críticamente enfermo.
El gasto de energía del paciente críticamente enfermo, varia ampliamente durante el transcurso de la enfermedad grave. Se considera que, durante la fase aguda temprana, el consumo de energía disminuye para después aumentar gradualmente durante la fase aguda tardía, hasta llegar a ser mayor al de un paciente sano de las mismas características.
Posteriormente, en la fase crónica o de recuperación disminuye nuevamente. Existen diferentes eventos que pueden alterar el gasto energético, incluyendo la fiebre, la hipotermia, los cambios en la frecuencia cardíaca (FC), la agitación, la sedación, los betabloqueadores no selectivos, entre otros.
El metabolismo de los macronutrientes en el paciente crítico presenta múltiples alteraciones durante la enfermedad. La oxidación de los macronutrientes incrementa de manera significativa, principalmente la de los carbohidratos, de manera temprana, para cambiar a un aumento del empleo de lípidos y proteínas en la fase tardía.
La glucosa es el principal sustrato energético en la enfermedad crítica temprana. El cuerpo moviliza rápidamente las reservas de glucógeno, junto con un aumento de la producción endógena a base de lactato, glicerol y alanina a nivel del riñón, el intestino y el hígado. Este estado, francamente catabólico, se ha visto correlacionado con la incapacidad de abolir la producción endógena de glucosa, pese a la administración de nutrientes externos y de insulina.
La alimentación temprana agresiva puede contribuir a la sobrealimentación en los primeros días de enfermedad, razón por la que las guías actuales recomiendan un escalamiento gradual de la nutrición. En un estado de estrés como la enfermedad crítica, las proteínas de fase aguda ven su síntesis aumentada y aquellas involucradas en la respuesta inmune aumentan para favorecer la recuperación.
Esto se ha visto acompañado de una disminución significativa de la musculatura esquelética que condiciona debilidad e incapacidad física en el período posterior a la enfermedad crítica por aumento de la destrucción muscular esquelética sin un aumento concomitante en la síntesis durante el período de agresión fisiológica. Esto proveerá de aminoácidos esenciales para la respuesta inmune inicial, tanto los elementos estructurales como el material para la oxidación y la energía, con creación de material de desecho en la forma de amonio y nitrógeno. Se tendrá como consecuencia un balance negativo de nitrógeno y la depleción gradual de las reservas corporales.
Los lípidos presentan un aumento en su metabolismo durante la enfermedad crítica también, pero en una menor magnitud que los carbohidratos. Los triglicéridos endógenos, mantenidos en los adipocitos, y los triglicéridos exógenos, liberados de los quilomicrones y otras lipoproteínas, se hidrolizan para obtener ácidos grasos libres y glicerol. La oxidación de los ácidos grasos libres está aumentada en los tejidos periféricos, como una alternativa de energía; sin embargo, el empleo pleno de esta fuente de energía requiere de mitocondrias funcionales.
La capacidad de las células para transportar los ácidos grasos de cadena larga desde el citosol a las mitocondrias se ve afectada. Esto conduce a la acumulación de estos en el interior de las células, lo que produce una inhibición de la función de la enzima piruvato deshidrogenasa (PDH) con la subsiguiente acumulación de piruvato, lactato y la acidosis intracelular.
Esta es una de las causas de la disminución de la respiración aeróbica. En las últimas fases de una enfermedad crítica, la oxidación de los ácidos grasos puede ocurrir en los tejidos periféricos, mientras que, en el hígado, se convierten en cuerpos cetónicos o se re-esterifican en triglicéridos y se liberan en el torrente sanguíneo como lipoproteínas de muy baja densidad (VLDL) e incrementan su nivel circulante.
El paciente crítico padece una serie de modificaciones fisiológicas que son susceptibles de ser moduladas mediante la intervención nutricional. La comprensión de los mecanismos fisiopatológicos ayuda a comprender cómo la terapia nutricional mejora el pronóstico de los pacientes, en los que una intervención temprana y adecuada para el contexto del paciente puede mejorar su pronóstico a corto y largo plazo.
Referencias
- Compher C, Bingham AL, McCall M, et al. Guidelines for the provision of nutrition support therapy in the adult crítically ill patient: The American Society for Parenteral and Enteral Nutrition. JPEN J Parenter Enteral Nutr. 2022; 46(1):12-41.
- Singer P, Blaser AR, Berger MM, et al. ESPEN guideline on clinical nutrition in the intensive care unit, Clin. Nutr. 2019;38(1):48-79.


















